Что вызывает гемобартонеллез у кошек?
Обычно возбудителем гемобартонеллеза у кошек являются микоплазмы вида Mycoplasma haemofelis (прежнее название — Haemobartonella felis), паразитирующая в крови на поверхности эритроцитов. Кошки могут заражаться также дугой разновидностью — Mycoplasma haemominutum, но случается это гораздо реже. Микоплазмы — это микроорганизмы, занимающие промежуточное положение в медицинской классификации между бактериями, грибами и вирусами. Это самые маленькие самостоятельно существующие из известных микроорганизмов. Обе разновидности, и Mycoplasma haemofelis, и Mycoplasma haemominutum называют терминами «гемотропная микоплазма» или просто «гемоплазма», так как они крове(hemo)- ассоциированные(tropic).
Гемобартонеллез собак и кошек
Гемобартонеллёз – это заболевание кошек и собак, основным симптомом которого является анемия, вызываемое одноклеточным паразитом Mycoplasma haemofelis у кошек и Mycoplasma canis у собак. Заболевание более характерно для кошек, особенно для тех, кто имеет доступ на улицу. Собаки болеют редко, обычно это животные с удаленной селезенкой, а также имеющие тяжелые заболевания иммунной системы.
Паразит прикрепляется к мембране эритроцита (красной клетки крови) и вызывает ее повреждение, в результате чего эритроцит разрушается. Это приводит к анемии, то есть недостатку красных кровяных телец в организме.
Mycoplasmahaemofelis и M. haemocanis (ранее называли haemobartonellafelis и h. canis) – гемотропные микоплазмы, занимающие промежуточное положение между бактериями и риккетсиями. В настоящее время они классифицируются в пределах рода Mycoplasma в семействе бактерий Mycoplasmataceae. Они паразитируют на эритроцитах и приводят к их разрушению, то есть гемолитической анемии. Микоплазма имеет очень маленькие размеры (в несколько раз меньше размеров эритроцита), в мазках крови имеет форму маленьких шариков или палочек, размножается только в клетках организма (попытки культивировать её в лаборатории не увенчались успехом).
Заболевание может протекать как в острой форме и приводить к гибели животного, так и переходить в хроническую форму. Хроническая форма не связана со значительной анемией, также существуют кошки-носители, у которых нет признаков анемии.
Патогенез
Гемобартонеллёз относится к трансмиссивным заболеваниям, то есть передаётся через укусы кровососущих насекомых – блох, клещей. Особенно часто гемобартонеллёзом болеют уличные коты, что также говорит о том, что возможна передача через раны, полученные во время драк. Подвержены заболеванию и старые животные, а также кошки с ослабленной иммунной системой и имеющие какое-либо заболевание – например, вирусный лейкоз или иммунодефицит. Переливание крови также является потенциальным путём передачи данного заболевания. Инкубационный период, в течение которого происходит размножение микоплазм, но ещё нет клинических проявлений, может занимать от 8 до 14 дней (по некоторым источникам, до 34 дней).
После этого наступает острая фаза инфекции, которая характеризуется выраженной паразитемией (паразиты находятся в крови, на мембранах эритроцитов). Зараженные эритроциты могут терять свою двояковыпуклую форму, что нарушает их свойства, приводит к их разрушению, что и называется гемолитической анемией. Заражённые и разрушенные эритроциты утилизируются селёзенкой, что приводит к ее увеличению.
Гемолитическая анемия, как правило, сопровождается выраженным регенераторным ответом, исключая случаи, когда есть заболевание, приводящее к иммунодефициту. Кроме того, при гемобартонеллезе имеет место иммуноопосредованный компонент анемии. Он заключается в появлении антител, которые «помечают» эритроциты для их дальнейшей утилизации, и среди этих «помеченных» могут быть и здоровые эритроциты, которые уничтожаются клетками иммунной системы.
Клинические признаки
У здоровых кошек заболевание может вызывать развитие острой формы. При этом здоровые собаки редко болеют в острой форме. Основные признаки заболевания связаны с анемией и не являются специфическими: вялость, слабость, сниженный аппетит, бледность слизистых оболочек, потеря веса, обезвоживание, а также может наблюдаться лихорадка.
Диагностика
Выявить данное заболевание можно путем лабораторной диагностики. Есть два основных метода лабораторной диагностики: микроскопия мазка крови и ПЦР крови. Первый метод не всегда позволяет выявить микоплазму, особенно при хроническом течении и малом количестве паразита. Поэтому более точная диагностика осуществляется с помощью метода ПЦР (полимеразной цепной реакции) – выявление ДНК микроорганизма в крови животного.
Лечение и профилактика
Без лечения смертность при острой форме инфекции может достигать 30%. Лечение комплексное и зависит от тяжести заболевания. Используют антибиотики тетрациклинового ряда, которые назначаются длительным курсом, а также препараты для борьбы с анемией, витамины, глюкокортикоидные препараты, в тяжелых случаях требуется переливание крови. Недолеченные кошки, которые выздоравливают, как правило, остаются носителями всю жизнь.
Вакцинации от гемобартонеллёза не существует. Чтобы обезопасить своё животное от заражения гемобратонеллёзом, достаточно регулярно обрабатывать его любыми препаратами против блох и других кровососущих насекомых.
Ветеринарный врач, специалист УЗД, Берлизова Алина Михайловна
Как передаются Mycoplasma haemofelis и Mycoplasma haemominutum?
Клещи и блохи заражаются этими микоплазмами при паразитировании на больных животных. Когда клещ(или блоха) оказывается на кошке и кусает ее, микоплазмы попадают в кровь, передавая болезнь. Так как микроорганизмы живут в клетках крови, они могут распространяться при переливании крови от инфицированного животного здоровому. У кошек микоплазмы могут также передаваться котятам от кормящей кошки с молоком. Болезнь может также распространяться через укусы других кошек — животные, выходящие на улицу, подвержены более высокому риску заражения. В грппе риска находятся также котята в возрасте до полугода.
Пути заражения
Гемобартонеллез у кошек развивается и распространяется в организме при значительном нарушении в работе иммунной системы. Клеточная защита играет важную роль в механизме противостояния инфекционной анемии.
После того, как возбудитель проникает в организм кошки, вредоносные микроорганизмы начинают активно увеличивать свою колонию, поражая красные кровяные тельца и клеточные структуры печени, лимфатических узлов, костного мозга и селезенки.
Гемобартонеллы крепятся к эритроцитам, постепенно приводят к повреждению оболочки, изменяя химические и физические свойства на клеточном уровне. Свойства транспортировки кислорода эритроцитами нарушаются, а сами красные кровяные тельца быстрее погибают (средняя продолжительность существования эритроцита – 120 дней).
Пораженные гемобартнеллами клетки нагружаются специфическими антителами и быстрее подвержены фагоцитозу.
Инфекционная анемия с преобладанием пораженных красных кровяных телец всегда сопровождается нарушениями и изменениями в организме. Прежде всего страдают селезенка и печень, отмечается их увеличение в объемах. Но малокровие начинает развиваться только в тех случаях, когда системы кроветворения перестают справляться со своими функциями. Таким образом, симптомы гемобартенеллеза у кошек развиваются с началом поступления незрелых красных кровяных телец в системный кровоток.
Причинами диатезных геморрагий и дистрофий органов из паренхиматозных тканей становиться недостаток в них кислорода. Гипоксия тканей приводит к нарушениям трофики в клетках, нарушая равновесие кислотно-щелочного баланса. Это сопровождается ацидозом, экскретированием гемоглобина в урину (моча приобретает красный или темно-коричневый цвет).
Заразиться гемобартенеллезом домашние кошки могут несколькими путями:
- укусы зараженных животных;
- укусы кровососущих насекомых;
- через фето-плацентарный барьер (от зараженной матери через плаценту к плодам);
- при родовом процессе через родовые пути и с молоком при лактации;
- во время переливания крови от больного животного.
При нарушениях обменных процессов в организме на фоне прогрессирующего гемобартенеллеза, развивается общее отравление, процессы воспалительного характера и кровоизлияния. Симптомы заболевания у пораженных животных характеризуются лихорадочными состояниями, нарушениями работы сердца и пищеварительной системы.
Не смотря на высокую заразность, гемобартонеллез кошек не заразен для людей и встречается только у кошек. Существует предположение, что вирус лейкемии кошек играет важную роль в развитии инфекционной анемии. В пораженном вирусом лейкоза организме легче развиваются микоплазмы, так как возникает иммуносупресия.
Симптомы гемобартонеллеза у кошек.
У кошек гемобартонеллез может протекать легко, беcсимптомно, лишь с легкой анемией, так и в очень тяжелой форме. Признаки заболевания — депрессия, потеря аппетита, дегидрация. В тяжелых случаях, выраженная анемия может проявляться в потере веса, побледнению слизистых оболочек, слабости, учащенном сердцебиении и дыхании, желтухе, и даже приводить к смерти кошки. Некоторые владельцы замечают, что кошки начинают есть мусор или грязь. Кошки, зараженные вирусом кошачьей лейкимии (Feline Leukemia Virus, FeLV) подвержены более тяжелым формам гемобартонеллеза. Без своевременной терапии некоторые кошки могут погибнуть от тяжелой анемии.
Иногда кошка может выздороветь, но остаться носителем гемобартонеллеза. В этом случае кошка выглядит полностью здоровой, но в её крови присутствует некоторое количиство микоплазмов. Если кошка попадает в стрессовую ситуацию, микоплазмы могут размножиться и вызвать повторное заболевание.
Уход за больным животным
Заболевшего инфекционной анемией питомца не нужно изолировать в отдельной комнате, т. к. болезнь не заразна. Лежанку относят в тёплое и тихое место, чтобы обеспечить животному покой. Туалетный лоток не перемещают, но следят за тем, ходит ли в него питомец. Животное может мочиться под себя от слабости, поэтому заранее готовят второе спальное место.
Рекомендуем прочитать: Обзор препарата для иммуностимуляции кошек Фоспренил
Для ускорения выздоровления нужна диета, содержащая особое, гемовое железо (содержится в продуктах животного происхождения). Вещество является основой формирования гемоглобина у всех млекопитающих. Количество пищи — не менее 200 граммов для взрослого животного в сутки.
Состав рациона при лечении гемобартонеллёза:
- говяжье мясо и печень;
- свиные лёгкие и сердце;
- кровь крупного рогатого скота.
Не имеет значения, в сыром или варёном виде дают корм. Важно, чтобы продукты не замораживались перед приготовлением. В этом случае мясная пища сохраняет все полезные свойства. При полном отказе от еды владельцу приходится кормить кота принудительно.
Борьба с животным лишь сильнее ослабит его, поэтому предпочтительнее внутривенное питание белковым гидролизатом в условиях стационара.
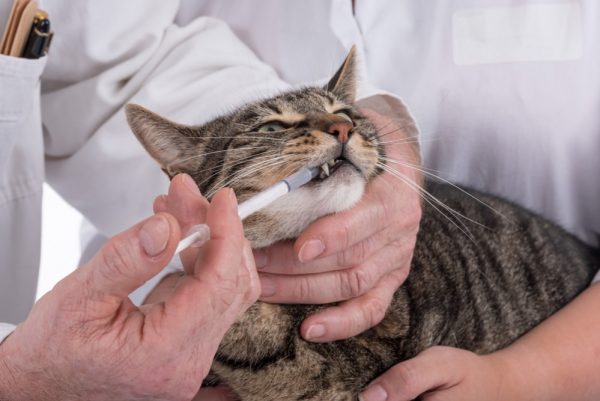
Измученный болезнью питомец не вылизывается, поэтому владелец берёт на себя уход за его шерстью. Её осторожно вычёсывают и увлажняют при необходимости. Больше сложностей возникает, если приходится часто давать коту таблетки (капсулы). От измельчённого в порошок лекарства, смешанного с кормом, животное отказывается. Поэтому применяют приспособление под названием таблеткодаватель, или пиллер. С его помощью кладут драже или таблетку коту прямо в рот вместе с бульоном или водой, чтобы облегчить глотание.
Приём лекарств с таблеткодавателем облегчает процесс лечения кошки от гемобартонеллёза
Действует устройство как шприц, спасая пальцы человека от царапин и укусов больного животного. Ветеринары всегда помогут владельцу научиться правильно пользоваться пиллером.
Диагностика гемобартонеллеза у кошек.
Иногда микроорганизмы можно обнаружить в мазке крови внутри клеток. Чтобы их найти капля крови размазывается по предметному стеклу, окрашивается и исследуется под микроскопом. Количество микроорганизмов в крови может значительно колебаться. Можно обнаружить множество микоплазмов в одном образце, и ни одного в образце, взятом через два часа. Анализ крови с использованием методомполимеразной цепной реакции (ПЦР) позволяет точно определить, заражена ли кошка гемотропным микоплазмозом.
№AN405КРО, Исследование на наличие кровепаразитов
Микроскопия мазка крови является одним из методов диагностики векторных (трансмиссивных заболеваний), зачастую на приеме в клинике. Наиболее распространенные из них: анаплазмоз, эрлихиоз, бабезиоз, гепатозооноз, цитозооноз кошек, дирофиляриоз, гематропные микоплазмозы. Реже чума собак, токсоплазмоз, лейшманиоз.
- Подготовка пациента
- Показания и противопоказания
- Интерпретация и форма выдачи результата
Возможные находки при окраске мазка – вирусные и бактериальные включения, тельца Жолли, и др.
Анаплазмозы ‒ это трансмиссивные заболевания, которые вызываются Anaplasma phagocytophilum и Anaplasma platys ‒ грамотрицательными внутриклеточными паразитическими протобактериями, принадлежащими семейству Anaplasmataceae.
Основными переносчиками A. phagocytophilum являются клещи комплекса Ixodes ricinus-persulcatus. В Европе основным переносчиком являются клещи Ixodes ricinus, а в России и Азии ‒ Ixodes persulcatus и Dermacentor silvarum.
A. phagocytophilum передается между разными стадиями клеща (от личинки нимфе и далее имаго), но не трансовариально (от имаго ‒ яйцам). Заражение собак и кошек происходит при питании на них инфицированных нимф или имаго клещей, которые, в свою очередь, заражаются при питании на диких животных-резервуарах. Инфицирование возможно, если клещ находится на животном в прикрепленном состоянии в течение 36-48 часов. После попадания A.phagocytophilum в кровяное русло микроорганизм прикрепляется к поверхности нейтрофилов, а затем проникает в клетки путем эндоцитоза. A. phagocytophilum вызывает нарушение функции нейтрофилов, что определяет возможность выживания микроорганизма внутри данных клеток. A. phagocytophilum может поражать клетки костного мозга и мегакариоциты, однако их роль в патогенезе инфекции остается неясной.
Эрлихиозы ‒ это группа трансмиссивных заболеваний, которые вызываются внутриклеточными, грамотрицательными бактериями Ehrlichia canis, Ehrlichia ewingii и Ehrlichia chaffeensis и переносятся клещами. Бактерии образуют морулы в фагосомах циркулирующих лейкоцитов. Ehrlichia canis поражает моноциты и вызывает моноцитарный эрлихиоз собак (МЭС), который является одной из наиболее значимых инфекций домашних собак по всему миру. Ehrlichia ewingii поражает гранулоциты и вызывает гранулоцитарный эрлихиоз собак. Ehrlichia chaffeensis поражает мононуклеарные лейкоциты, вызывая моноцитарный эрлихиоз человека; собаки являются резервуарными хозяевами. Географическое распространение того или иного патогена обычно ограничено ареалом переносчиков и резервуарных хозяев.
Тяжесть клинических симптомов при эрлихиозе зависит от таких факторов, как размер инокулума, функционального состояния иммунной системы хозяина, вида и штамма микроорганизма и наличия сопутствующих инфекций. Клиническая картина может осложняться тем, что у разных микроорганизмов могут быть одни и те же переносчики, поэтому часто встречаются коинфекции такими патогенами, как Babesia spp. и Bartonella spp.
E. canis переносится преимущественно коричневым собачьим клещом (Rhipicephalussanguineus), инфекция встречается у собак в Азии, Африке, Америке, Европе. Существует несколько штаммов E. canis, которые отличаются вирулентностью. Личинки клещей заражаются при питании на инфицированных собаках. Возможна трансстадиальная передача инфекции E. canis (от личинки нимфе и имаго).
Очевидной возрастной или половой предрасположенности к МЭС у собак не наблюдается, однако данные, что немецкие овчарки более восприимчивы к заболеванию. Прогноз на исход заболевания у собак этой породы обычно менее благоприятный. У собак смешанных пород заболевание встречается реже. Была описана спонтанная инфекция E. canis у кошек в Северной и Южной Америке, однако клинический эрлихиоз у данного вида встречается редко.
Микроорганизм размножается в мононуклеарных фагоцитах путем бинарного деления; при разрушении инфицированных клеток происходит заражение здоровых клеток.
Микроорганизмы Ehrlichia и Anaplasma можно непосредственно наблюдать при окрашивании по Романовскому мазков периферической крови. Они выглядят как базофильные короткие палочки или плейоморфные коккобациллы размером от 0,2 до 1,0 мкм, обнаруживаемые поодиночке или в скоплениях внутри ограниченных мембраной клетки-хозяина цитоплазматических вакуолях, так называемых морулах. Различные микроорганизмы инфицируют преимущественно различные клетки крови, в том числе нейтрофилы и эозинофилы, лимфоциты и моноциты, а также тромбоциты (A.platys). Количество свободно циркулирующих микроорганизмов часто ниже предела выявления с помощью световой микроскопии. Вероятность выявления возбудителей возрастает при исследовании мазков лейкоцитарной пленки.
Бабезиоз (пироплазмоз) – это широко распространенное трансмиссивное заболевание, вызываемое кровепаразитами рода Babesia, переносчиками которого являются клещи. В зависимости от географического месторасположения, переносчиками бабезиоза могут быть Rhipicephalus sanguineus, Dermatocentor reticulatus, Haemaphysalis eliptica. Передача Babesia spp. происходит при укусе клеща-переносчика. Возможна прямая передача малой бабезии Babesia gibsoni при укусах с глубоким повреждением кожи (у бойцовых собак). На сегодняшний день классификация бабезиоза собак включает деление на большую и малую формы. B. сanis является наиболее распространенной большой бабезией и имеет три отдельных подтипа: B. сanis vogeli (распространена в Африке, Азии, Европе, Америке), B. canis canis (в Европе), B. canis rossi (в Африке). К малым бабезиям собак относят: B. gibsoni (встречается в Африке, Азии, Австралии, Европе, Америке), B. conradae (в Калифорнии), B. microti-like (в Северно-Западной Испании).
Бабезиоз кошек не изучался столь подробно, как бабезиоз собак. У кошек были обнаружены несколько видов малых бабезий, включая Babesia felis, B. cati и B. leo. Инфекция обычно встречается у животных в возрасте до трех лет, породной или половой предрасположенности не наблюдается. Виды больших бабезий также могут вызывать болезни у кошек.
Патогенность бабезий определяется, главным образом, видом и штаммом микроорганизма. В патогенезе заболевания играют роль возраст инвазированного животного и характер иммунного ответа. Цикл развития бабезий протекает в эритроцитах собак или кошек. После деления дочерние формы бабезий выходят из эритроцитов, разрушая их, и проникают в еще не зараженные красные клетки крови. Цикл размножения повторяется. Две основные формы Babesia, большие и мелкие формы, могут быть идентифицированы микроскопически.
Паразиты могут выглядеть в мазке крови как светло-голубые микроорганизмы парной каплевидной формы внутри эритроцита, имеющие темно-фиолетовое ядро (Babesia canis) или как тонкие кольца с эксцентрично расположенным фиолетовым ядром (в виде кольца-перстня), например B.gibsoni.
Нутталлиоз лошадей (nuttalliosis) — это пироплазмидоз, характеризующийся повышением температуры, угнетенностью общего состояния, анемией, желтушностью слизистых оболочек, нарушением сердечно-сосудистой и пищеварительной систем. Нутталлиоз лошадей имеет более широкое распространение на юге страны, вызывается кровопаразитом Nuttallia equi из сем. Piroplasmatidae.
Нутталлия характеризуется разнообразием форм и неодинаковой величиной. Преобладают в мазках крови округлые формы (круглая и кольцевидная). Две груши, соединенные узкими концами вместе, практически в эритроцитах отсутствуют. Характерная форма нутталлий — крестовидная, напоминающая «мальтийский крест», который образуется при делении нутталлий почкованием. По величине нутталлий в эритроцитах подразделяются на крупные (равны радиусу эритроцита), средние (половине радиуса эритроцита) и мелкие ( меньше радиуса эритроцита). Мелкие нутталлии обычно обнаруживают в эритроцитах у лошадей-нутталлионосителей, а также при хронической форме болезни.
Гепатозоонозы — согласно таксономической классификации в род Hepatozoon (семейство Hepatozooidae) объединены более 300 видов паразитов, обитающих в организмах позвоночных. Жизненный цикл Hepatozoon canis гетерогенен, их переносчиками служат кровососущие беспозвоночные, в том числе аргасовые и иксодовые клещи (Rhipicephalus sanguineus). Собаки заражаются гепатозоонозом при присасывании зараженного клеща, при травмах кожных покровов, при поедании более мелких животных, пораженных клещами с возбудителем. Могут болеть и кошки. При попадании в организм животного спорозоиты гематогенным путем разносятся в ткани органов-мишеней, где поглощаются фагоцитами и мигрируют в различные ткани. Первоначальная мерогония отмечается в печени, в кишечной лимфатической ткани и в брыжеечных лимфатических узлах. Основная точка мегогонии – клетки костного мозга. Меронты H. canis встречаются в клетках мышечной ткани, образуя характерное морфологическое «колесико», то есть мерозоитов расположенных в меронтах.
H. canis способен вызывать воспалительные скелетные поражения: поражения надкостницы и периостит. Кроме того, высокая пораженность животных проявляется лихорадкой, летаргией, анемией и истощением. Часто может протекать бессимптомно. Особенно тяжело протекает такая форма при коинфицировании эрлихиями, бабезиями и другими возбудителями трансмиссивных инфекций. Как правило, при заражении.
С использованием микроскопических методов гематоциты Hepatozoon довольно часто диагностируются в нейтрофилах.
В условиях клиники диагностика может быть осуществлена путем обнаружения гамонтов в крови (окрашенный мазок). Однако, чувствительность такого метода крайне низка. Повысить чувствительность исследования можно путем получения концентрата белых клеток крови с помощью седиментации в гематокритном капилляре с последующей окраской выделенного слоя лейкоцитов.
Цитозооноз – трансмиссивное инфекционное заболевание с широким диапазоном географического распространения. Возбудитель — гемопротозойный паразит Cytauxzoon felis, который передается векторным путем ( иксодовые клещи Dermacentor variabilis и Amblyomma americanum, Amblyomma cajennense и др. ) . Относится к отряду Piroplasmida, семейству Theileriidae.
Хотя C. felis является видом, наиболее распространенным среди домашних кошек в США, это только один из нескольких видов из рода Cytauxzoon.
Заражение C. felis или близкородственными простейшими , встречается у широкого круга диких видов кошачьих. Предполагаемый резервуар-хозяин, который обитает в Соединенных Штатах рысь (Lynx rufus rufus), а также крупные и дикие крупные кошки.
Больные и здоровые кошки могут жить вместе без передачи возбудителя при отсутствии вектора. Паразит может присутствовать в организме в двух формах – неэритроцитарной (стадия шизонта) и эритроцитарной (пироплазмы).
Заболевание наблюдается у кошек разного возраста и пола. Породной предрасположенности нет.
В жизненном цикле C. felis половая фаза размножения происходит в кишечнике клеща . Оокинеты выходят из кишечника, попадают в полости организма и мигрируют в слюнные железы, где они размножаются как инфекционные спорозоиты. После того, как они попадают в организм хозяина во время проглатывания клеща , они проникают и развиваются, прежде всего, внутри фагоцитов. Они сначала визуализируются как нечеткие везикулярные структуры в цитоплазме инфицированных клеток и позже, как большие, отчетливые, ядерные шизонты, которые активно подвергаются делению по шизогонии и бинарному делению. Созревшие шизонты отпочковываются (мерозоиты) и в конечном счете, заполняют всю клетку хозяина. Фагоциты заполняют просветы сосудов практически в каждом органе , вплоть до образования тромбов.
Клетка-хозяин, разрушаясь , высвобождает мерозоиты в кровь или тканевую жидкость. Мерозоиты появляются в макрофагах, а через 1-3 дня после этого они наблюдаются в эритроцитах. Затем они внедряются в незараженные эритроциты и вызывают паразитемию поздней стадии, которую можно обнаружить при микроскопии мазков крови , обычно от 1 до 3 дней до клинической болезни.
В мазке крови Cytauxzoon felis похож на Babesia gibsoni, мелкие одиночные включения в виде кольца (перстня) с небольшим темным ядром внутри эритроцита.
Dirofilaria immitis и Dirofilaria repens – паразитические нематоды, принадлежащие надсемейству Filarioidea. Окончательными хозяевами паразитов являются собаки, в редких случаях – кошки. Кроме собак, заражению повержены лисы, волки, койоты, дикие кошки, хорьки, ондатры, носухи, морские львы, а также люди. Промежуточными хозяевами являются комары родов Aedes, Anopheles и Culex.
После инокуляции 2-3 месяца личинки находятся в подкожной клетчатке и мышцах, за это время они два раза линяют.
Самки выделяют в кровеносное русло личинок – микрофилярий, которые могут жить в кровеносных сосудах внутренних органов в течение нескольких месяцев. Это личинки первой стадии, их еще называют «личинки стадии L1». При питании комаров на инвазированных животных микрофилярии попадают в организм насекомых, где в течение примерно двух недель происходит их последующее развитие до стадии L3. Во время укуса комара инвазионные личинки проникают в организм окончательного хозяина, после чего мигрируют в подкожную клетчатку и мышцы. В течение последующих нескольких месяцев личинки дважды линяют, проходя стадии развития L4 и L5. Стадия L5 – незрелые взрослые особи гельминтов, достигающие длины 1-2 см. Юные особи D. repens остаются паразитировать в пределах подкожной клетчатки, иногда подвергаясь атипичной миграции (в глаза, нервную систему и др.). Особи D. immitis мигрируют в системный кровоток и током крови заносятся в легочные артерии. Как правило, через 7-9 месяцев после начала инвазии в крови циркулируют микрофилярии. Продолжительность жизни гельминтов в организме собаки может достигать семи лет от момента заражения. Юные и взрослые особи D. immitis локализуются преимущественно в каудальных легочных артериях, иногда мигрируя в главные легочные артерии, при тяжелой инвазии – в правые отделы сердца и крупные вены.
Dirofilaria repens вызывает кожную форму дирофиляриоза. Взрослые черви, достигающие длины 15 см, локализуются в подкожной клетчатке. Жизненный цикл сходен с таковым D. immitis. Продолжительность препатентного периода составляет 6-8 месяцев. Инвазия обычно протекает в субклинической форме, в некоторых случаях может развиваться дерматит, сопровождающийся локальной алопецией, зудом, эритемой и образованием корочек.
У лошадей возможно обнаружить в мазке крови микрофилярий круглых гельминтов Setaria equina семейства Filariidac подотряда Filariata, которые вызывают заболевание сетариоз лошадей. Половозрелые сетарии паразитируют в брюшной и грудной полостях, печени, перикарде и других органах, личинки — в крови. Преимагинальные стадии развития могут проникать в переднюю камеру глаза. Сетарии — биогельминты. Промежуточными хозяевами являются кровососущие комары родов Aedes и Culex. Известно, что личинки паразита циркулируют в крови лошадей и мулов. Максимальное их количество в периферической крови наблюдается вечером, когда происходит активизация комаров и нападение их на животных для кровососания. В организме насекомых личинки развиваются в грудных мышцах, а потом мигрируют к хоботку. За 12 — 16 суток они становятся инвазионными. Заражение непарнокопытных животных происходит во время нападения на них для кровососания инвазированных промежуточных хозяев. Паразиты достигают половой зрелости в организме лошадей в течение 8 — 10 мес.
При микроскопии окрашенного мазка микрофилярии трудно идентифицировать до вида или рода.
Гемотропные микоплазмозы — гемоплазмы – это мелкие (0,3-0,8 мкм) некультивируемые микроорганизмы, которые локализуются на поверхности эритроцитов и вызывают гемолитическую анемию различной степени тяжести у инфицированных животных. Гемоплазмы поражают широкий круг млекопитающих, включая человека, распространены повсеместно.
Минимум три вида гемоплазм вызывают инфекции у домашних и диких кошек: Mycoplasma haemofelis, Candidatus Mycoplasma haemominutum и Candidatus Mycoplasma turicensis. M. haemofelis (ранее называемая штаммом из Огайо, или крупной формой Haemobartonella felis) является наиболее патогенным организмом, вызывающим гемолитическую анемию от умеренной до выраженной у иммунокомпетентных кошек. Данное заболевание называется инфекционной анемией кошек. При цитологическом исследовании мазков крови M. haemofelis имеют форму кокков, иногда образующих цепи по три-шесть микроорганизмов.
Ca. M. haemominutum (ранее называемая калифорнийским штаммом, или малой формой H. felis) обычно меньше, чем M. haemofelis. Связи между инфицированием данным организмом и заболеванием у иммунокомпетентных кошек установлено не было. При цитологическом исследовании мазков крови Ca. M. haemominutum обнаруживаются как кокки малого размера, от 0,3 до 0,6 мкм в диаметре. Однако достоверно отличить M. haemofelis от Ca. M. haemominutum с помощью данного метода невозможно. Ca. M. haemominutum встречается у кошек по всему миру, инфекции наблюдаются у 20% кошек, поступающих на прием в ветеринарные госпитали. Инфекция Ca. M. haemominutum у кошек вызывает незначительное снижение гематокрита. У кошек с коинфекцией FeLV и Ca. M. haemominutum отмечается более выраженная анемия, чем при моноинфекции Ca. M. haemominutum, а прогрессирование миелопролиферативного заболевания, вызванного FeLV, происходит быстрее.
Несколько видов гемоплазм могут поражать собак. У собак, которым была проведена спленэктомия, и в редких случаях при наличии иммуносупрессивных патологий или коинфекций, наблюдается гемолитическая анемия при инфекции Mycoplasma haemocanis (ранее называемой Haemobartonella canis). M. haemocanis представляет собой микроорганизм округлой формы, зачастую формирующий длинные цепи. Распространенность данной инфекции особенно высока у собак, выращенных в питомниках, у которых часто отмечается субклиническая форма болезни.
У собак было обнаружено еще три вида гемоплазм. Candidatus Mycoplasma haematoparvum представляет собой микроорганизм небольшого размера (0,3 мкм) округлой формы, имеющий морфологическое и генетическое сходство с C.. Mycoplasma haemominutum.
Пути передачи инфекции гемоплазм остаются неясными.Очевидно, блохи и другие членистоногие могут играть роль в передаче инфекции гемоплазм у кошек, однако данные экспериментальных исследований по данному вопросу недостаточно убедительны.
M. haemofelis и C. M. haemominutum — оба эти гемопаразита прикрепляются к поверхности эритроцита, при этом C. M. haemominutum является меньшим из двух микроорганизмов, и обычно выглядит в форме темного стержня на поверхности эритроцита.
M. haemofelis большего размера и может образовывать отчетливые тела в виде кольца , которые можно увидеть на эритроцитах в мазке крови. Часто, только один из этих простейших обнаруживают в мазке крови. Некоторые кошки могут быть заражены обоими видами.
Чума плотоядных- острая контагиозная вирусная болезнь домашних собак и диких животных (многих видов отряда хищных), имеющая большое ветеринарное значение. Заболевание вызывается вирусом чумы плотоядных (Canine Distemper Virus, CDV), который является оболочечным, плеоморфным РНК-содержащим вирусом, принадлежащим роду Morbillivirus (семейство Paramyxoviridae). CDV родственен вирусу кори и вирусу чумы крупного рогатого скота и использовался в качестве модели при изучении патогенеза кори. Вирусная оболочка состоит из трех белков: гемагглютинина (Н), белка слияния (F) и матриксного белка (М). Именно Н-белок играет определяющую роль в присоединении вируса к клеткам и проникновении в них. Инфекция у собак может протекать в форме тяжелого заболевания, поражающего различные системы организма ‒ пищеварительную, респираторную и нервную.
Хорьки восприимчивы к заболеванию, в то время как у кошек оно не встречается. Вирус, выделяемый дикими животными (например, енотами), может поражать домашних собак, а вирус, выделяемый домашними собаками, представляет значительную опасность для диких животных, вызывая вспышки заболевания с высоким уровнем смертности. Вирус чумы плотоядных также является одним из патогенов, вызывающих комплекс респираторных инфекций собак (КРИС).
На ранних стадиях заболевания цитоплазматические тельца-включения, содержащие вирус, можно обнаружить в небольшом количестве циркулирующих лимфоцитов и в единичных моноцитах, нейтрофилах и эритроцитах. Включения крупные (до 3 мкм), округлой или овальной формы, различные по цвету – от синевато-серого до пурпурного. Выявление клеток с включениями более вероятно, при исследовании препаратов лейкоцитарной пленки.
Сроки исполнения: 1 день ( плюс 1-2 дня для регионов).
Исследуемый аналит: цельная кровь.
Метод исследования: микроскопия мазка.
Подготовка пациента, показания и противопоказания: Специальной подготовки животного не требуется.
Показания:
- Лихорадка;
- анемия (обычно регенеративная);
- тромбоцитопения;
- гиперглобулинемия;
- спленомегалия;
- желтуха и пигментурия;
- скрининг при выборе донора крови или при подборе животных для разведения;
- лимфаденопатия.
Противопоказания: не известны.
Метод отбора биоматериала: венепункция периферической вены.
Преаналитика: взятие крови — пробирка с розовой крышкой (с ЭДТА)0,5 мл; для крупных собак можно использовать пробирку с сиреневой крышкой (с ЭДТА) 2 мл. Заполнить пробирку кровью СТРОГО до отметки на этикетке. Осторожно перевернуть пробирку 7-10 раз для перемешивания крови с антикоагулянтом.
Стабильность пробы: 3 дня при +2°С…+8° С.
Интерпретация результата: в норме кровепаразиты не обнаруживают. Отсутствие кровепаразитов в мазке крови не исключает наличия инфекции.
Результаты исследования содержат информацию исключительно для врачей. Диагноз ставится на основании комплексной диагностики , в т.ч. ПЦР, ИФА или ELISA .
Форма выдачи результата: обнаружение / не обнаружение кровепаразитов .
Источники:
- Ш.Ваден,Д.Нолл, Ф. Смит, Л.Тиллей. Полное руководство по лабораторным и инструментальным исследованиям собак и кошек.
- «Гепатозооноз кошек» С.В. Коняев, Современная ветеринарная медицина, стр. 18-23, вып.1, 2021г.
- Green «Infections Diseas of the dog and cat».
- ATLAS OF CANINE AND FELINE PERIPHERAL BLOOD SMEARS Edition 1
Прогноз лечения гемобартонеллеза у кошек.
При отсутствии лечения велика вероятность гибели кошки (не менне 25%), при этом многие кошки после выздоровления остаются носителями, часто наблюдаются рецидивы заболевания. При наличии таких заболеваний, как хронические болезни почек, системные воспалительные реакции, вирусные инфекции и т.д. течение гемобартенеллеза значительно осложняется, что существенно ухудшает прогноз выживаемости кошки. При своевременном начале лечения гемобартонеллеза и сопутствующих заболеваний, вероятность выздоровления считается вполне реальной.